La patofisiología es la iencia que estudia las dolencias de una enfermedad.
Los orígenes de la enfermedad son desconocidos.
Se ha lanzado la hipótesis de que una infección viral u otro factor medioambiental en la niñez o durante el embarazo pueda preparar el sistema inmunológico para una reacción anormal más tarde. A nivel molecular, puede que exista una similitud estructural entre una agente infeccioso desconocido y componentes del sistema nervioso central, lo que causaría confusión más tarde en el sistema inmunológico (un proceso llamado mimenisto molecular). Con todo, aun no se conoce ningún virus de la esclerosis. Desde luego, la esclerosis múltiple no es contagiosa.
Se ha conseguido reconstruir el proceso del ataque del sistema inmunológico a la mielina a partir de observaciones en los tejidos dañados y el estudio de laEncefalomielitis Experimental Autoinmune (o EAE, de sus siglas en inglés), quPatrón IV: La lesión presenta bordes abruptos y oligodendrocitos degenerados, con un anillo de mielina. Ausencia de oligodendrocitos en el centro de la lesión. No está activado el complemento ni hay perdida de MAG.
Los dos primeros patrones se consideran ataques autoinmunes contra la mielina y los dos últimos contra los oligodendrocitos. Los dos primeros patrones son además similares a los producidos en EAE.
Las formas frontera de la esclerosis multiple también presentan lesiones incluidas en estos patrones. Así la neuromielitis óptica tendría lesiones mediadas por activación de complemento (patrón II). La esclerosis concéntrica de Baló mostraría pérdida de MAG según el patrón III y la EM progresiva primaria se correlacionaría con el patrón IV.
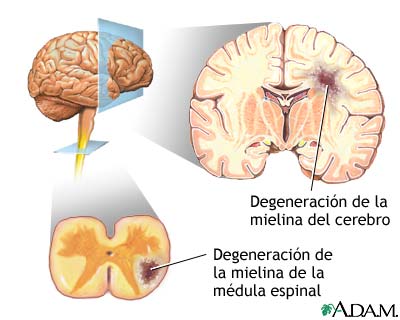
Desmielinización
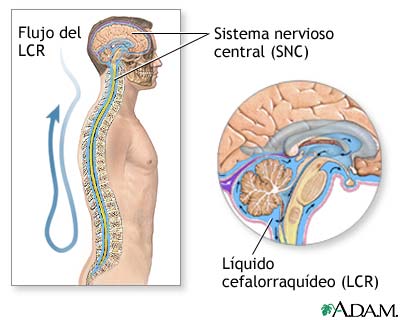
En estado normal, existe una barrera entre el sistema nervioso central y la sangre llamada barrera hematoencefálica, que está formada por células endoteliales tapizando las paredes de los vasos sanguíneos. En la esclerosis esta barrera se deteriora y células T autorreactivas la cruzan, provocando una proceso inflamatorio. La inflamación es facilitada por otras células inmunitarias y elementos solubles, como la citocina y los anticuerpos. A causa de este comportamiento anormal del sistema inmunológico, la esclerosis múltiple es considerada una enfermedad autoinmunitaria.
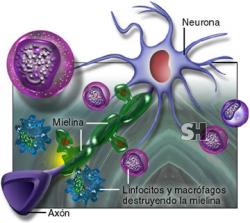
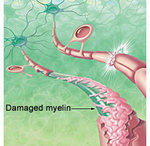
Ampliamente aceptado es que un subtipo especial de linfocitos, llamados Celulas CD4 -Th1-T, tienen una función clave en el desarrollo de la enfermedad. Bajo circunstancias normales, estos linfocitos pueden distinguir entre células propias y ajenas. En una persona con esclerosis múltiple, sin embargo, las células reconocen partes sanas del sistema central como ajenas y las atacan como lo harían con un virus. En la esclerosis, la parte atacada es la mielina, una sustancia grasa que cubre los axones de las células nerviosas y que es importante para una transmisión nerviosa adecuada.
La inflamación finalmente lleva a la apertura de la barrera hematoencefálica, lo que puede acarrear problemas como edemas. También causa la activación de macrófagos, de metaloproteinasas y otras proteasas y citocinas. Finalmente llevará a la destrucción de la mielina, proceso llamado desmielinización.
DAÑOS EN LOS AXONES
A través de la resonancia magnética y otros sistemas, se ha demostrado que el daño a los axones es una de los principales causas del desarrollo de discapacidades permanentes. Se ha demostrado que esta lesión interviene no sólo en formas crónicas o en estadios tardíos de la enfermedad, sino que está presente desde el inicio.
Los mecanismos que llevan a este tipo de daños no están explicados en su totalidad. Actualmente parece que una regulación anómala del glutamato así como la liberación de monóxido de nitrógeno (NO) tienen una función importante.
Varios experimentos en animales con EAE, encefalitis inducida, enfermedad supuestamente similar a la Esclerosis múltiple, han mostrado que a los que se les dieron medicamentos para la disminución de los niveles de glutamato en el cerebro tuvieron una disminución significativa en los daños a los axones.
Otra posibilidad es la destrucción directa de los axones por las células T autorreactivas.
Remielinización
Los oligodendrocitos originales que forman la cubierta de mielina no son capaces de recrear la cubierta una vez que ha sido destruida. Sin embargo, el cerebro es capaz de reclutar células madre que migran de otras zonas del cerebro desconocidas, se diferencian en oligodendrocitos maduros y recrean la cubierta de mielina. Esta nueva cubierta a menudo no es tan gruesa o efectiva como la original y ataques repetidos tendrán como reacción remielinizaciones cada vez menos efectivas, hasta que se forma una placa alrededor de los axones dañados. Las células madre se diferencian y remielinizan axones in vitro sin ningún problema, por lo que se sospecha que la inflamación o el daño al axón inhiben la diferenciación de las células madre in vivo.
La remielinización es una de las razones por las que, especialmente en la primeras fases de la enfermedad, los síntomas tienden a disminuir o desaparecer después de días a meses.
Resultado
Sin embargo, el daño a los axones y la pérdida irreversible de las neuronas aparecen muy pronto en el transcurso de la enfermedad. Los síntomas de la esclerosis son causados por lesiones múltiples en el cerebro y la espina dorsal y pueden variar mucho entre individuos, dependiendo de dónde ocurran las lePatrón IV: La lesión presenta bordes abruptos y oligodendrocitos degenerados, con un anillo de mielina. Ausencia de oligodendrocitos en el centro de la lesión. No está activado el complemento ni hay perdida de MAG.
Los dos primeros patrones se consideran ataques autoinmunes contra la mielina y los dos últimos contra los oligodendrocitos. Los dos primeros patrones son además similares a los producidos en EAE.
Las formas frontera de la esclerosis multiple también presentan lesiones incluidas en estos patrones. Así la neuromielitis óptica tendría lesiones mediadas por activación de complemento (patrón II). La esclerosis concéntrica de Baló mostraría pérdida de MAG según el patrón III y la EM progresiva primaria se correlacionaría con el patrón IV.